Existen algunas enfermedades minoritarias que afectan a un porcentaje muy bajo de la población y que todavía no tienen cura. La terapia génica es...
02/09/2012 00:27:23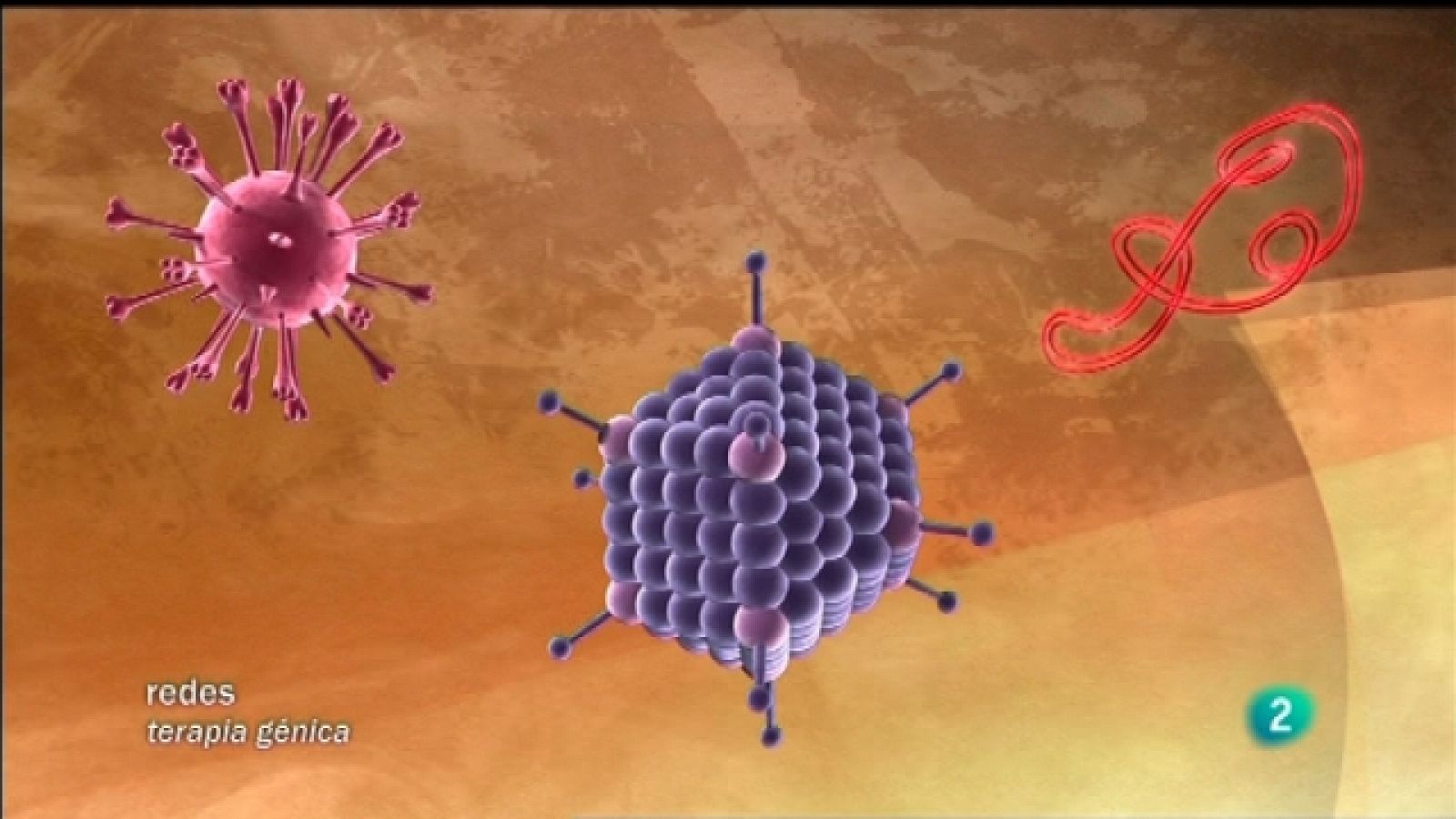

Existen algunas enfermedades minoritarias que afectan a un porcentaje muy bajo de la población y que todavía no tienen cura. La terapia génica es la gran promesa. En este capítulo de Redes, Punset entrevista a Fátima Bosch, experta en terapia génica de la Universidad Autónoma de Barcelona.
Bosch sostiene que la terapia génica es una herramienta eficaz para luchar contra enfermedades actualmente sin cura. Según ella, cuando su aplicación, haya desarrollado todo su potencial, algunas enfermedades hoy muy graves, se curarán como un simple resfriado.
Una de ellas sería la mucopolisacaridosis, una patología minoritaria, que afecta en un 50% a niños, en la que es experta Mercé Pineda, neuropediatra del Hospital Sant Joan de Déu de Barcelona. Además, recoge testimonios de familiares de enfermos, que ofrecen un punto de vista más cercano de cómo se vive con estas enfermedades.
Histórico de emisiones:
23/10/2011
- Dirigido por
- Eduard Punset
- Géneros
- Ciencia y futuro
- Idiomas
- Castellano
- Accesiblidad
- Subtitulado